Regulação do volume e da osmolaridade do ambiente interno do corpo
Atenção: o conteúdo deste site pertence à Universidade Federal de Viçosa.
A manutenção do ambiente interno, também denominado meio interno, é um dos princípios fundamentais da homeostase em mamíferos domésticos. Esse ambiente corresponde principalmente ao líquido extracelular (LEC), que envolve as células e garante condições físico-químicas adequadas para o funcionamento celular. O rim exerce papel central nesse controle ao regular, de forma precisa, o volume e a osmolaridade do LEC, ajustando continuamente a excreção ou a conservação de água e eletrólitos.
Essa função é particularmente relevante em animais terrestres, nos quais a ingestão de água e sais é variável. Assim, a arquitetura renal e seus mecanismos fisiológicos permitem respostas rápidas e coordenadas para evitar alterações volumétricas e osmóticas que comprometeriam a função celular.
O rim como órgão integrador da homeostase hidrossalina
Com frequência, os rins são lembrados apenas por sua função excretora. Entretanto, esse papel é parte de um processo bem mais complexo na integração da homeostase, sendo capaz de monitorar o estado do plasma e responder a sinais neurais e hormonais. Ao regular o volume sanguíneo, o rim sustenta a função cardiovascular; ao ajustar a osmolaridade plasmática, protege as células contra variações osmóticas que poderiam levar ao encolhimento ou edema celular.
Bases estruturais renais envolvidas na regulação
A regulação do volume e da osmolaridade depende de estruturas renais especializadas, cuja organização histológica sustenta funções regulatórias específicas.
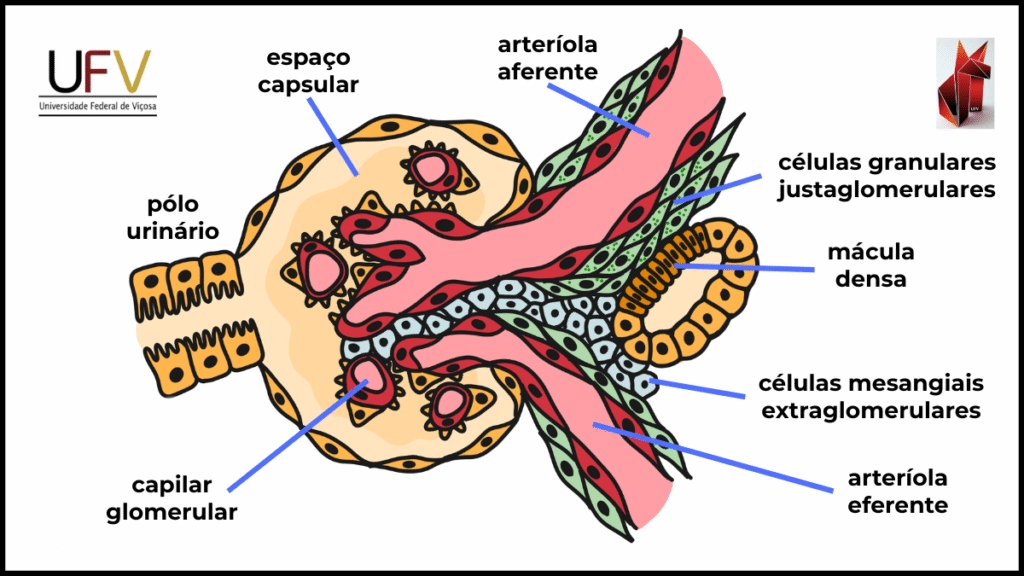
Aparelho Justaglomerular (AJG)
O aparelho justaglomerular localiza-se na região de contato entre o glomérulo e o túbulo distal. Ele é formado por:
Células justaglomerulares (granulares), localizadas na parede da arteríola aferente, especializadas na síntese e secreção de renina;
Mácula densa, segmento especializado do túbulo distal que detecta a concentração de Na+ no fluido tubular.
Essa proximidade estrutural permite que variações na composição do filtrado tubular sejam rapidamente traduzidas em ajustes na filtração glomerular e na liberação hormonal, exemplificando a integração estrutura-função no controle do volume do LEC.
.
Túbulos coletores e células principais
Os túbulos coletores, presentes no córtex e na medula renal, contêm as células principais, que representam o principal sítio efetor da regulação hidrossalina. Essas células expressam receptores para hormônio antidiurético (ADH) e aldosterona.
Do ponto de vista histológico, a presença desses receptores e de canais específicos de membrana permite que as células principais ajustem finamente a reabsorção de sódio e água, traduzindo sinais hormonais sistêmicos em respostas tubulares precisas.
Vasos retos e gradiente osmótico medular
Os vasos retos são capilares especializados que acompanham as alças de Henle dos néfrons justamedulares. Sua disposição paralela às alças permite a troca contracorrente, preservando o gradiente osmótico medular.
Essa organização vascular é essencial para que a medula renal permaneça hipertônica, condição indispensável para a reabsorção passiva de água nos túbulos coletores sob ação do ADH, demonstrando como a estrutura vascular sustenta diretamente a função de concentração urinária.
Barorreceptores intrarrenais
Os barorreceptores intrarrenais, localizados na arteríola aferente, detectam variações na pressão de perfusão renal. Quando essa pressão diminui, esses sensores estimulam a liberação de renina pelas células justaglomerulares, conectando diretamente a hemodinâmica renal ao controle hormonal do volume do fluido extracelular.
Mecanismos fisiológicos integrados de controle
Os sistemas fisiológicos responsáveis pela regulação do volume e da osmolaridade atuam de forma coordenada, embora cada um tenha um papel predominante.
Sistema renina-angiotensina-aldosterona (SRAA)
O SRAA é o principal regulador do volume do fluido extracelular.
O angiotensinogênio é uma glicoproteína plasmática produzida principalmente pelos hepatócitos e liberada continuamente na circulação. Ele constitui o substrato inicial do SRAA. Em situações como redução da pressão arterial, diminuição da perfusão renal ou queda da concentração de sódio na mácula densa, as células justaglomerulares do rim liberam renina, uma enzima proteolítica que cliva o angiotensinogênio, formando angiotensina I. Esta, por sua vez, é convertida em angiotensina II pela enzima conversora de angiotensina (ECA), expressa no endotélio vascular. Os pulmões são particularmente importantes nessa conversão, pois, além de expressarem ECA mais intensamente, a grande área de superfície capilar aumenta o contato da angiotensina I circulante com a enzima conversora. A angiotensina II é o principal peptídeo ativo do sistema, exercendo potente vasoconstrição, estimulando a liberação de aldosterona pela zona glomerulosa do córtex adrenal, além de aumentar a secreção de ADH e a sede. A aldosterona atua principalmente nas células principais do ducto coletor renal, promovendo maior expressão e atividade de canais de sódio (ENaC) e da Na⁺/K⁺-ATPase, favorecendo reabsorção de sódio e água e secreção de potássio, contribuindo para a restauração do volume extracelular e da pressão arterial.
Hormônio antidiurético (ADH)
O ADH é o principal regulador da osmolaridade plasmática. A elevação da osmolaridade é detectada por osmorreceptores hipotalâmicos, resultando na liberação do hormônio pela neuro-hipófise.
No rim, o ADH liga-se aos receptores V2 das células principais, promovendo a inserção de aquaporina-2 na membrana apical. Essa modificação estrutural transitória da membrana celular permite a reabsorção passiva de água para o interstício medular hipertônico, concentrando a urina e normalizando a osmolaridade do plasma.
Peptídeos natriuréticos atrial e cerebral (ANP e BNP)
Durante a expansão do volume circulante, os peptídeos natriuréticos atuam como antagonistas funcionais do SRAA e do ADH. O estiramento dos miócitos cardíacos desencadeia sua liberação, resultando em aumento da filtração glomerular e redução da reabsorção tubular de sódio. Esses hormônios agem diretamente sobre estruturas glomerulares e tubulares, promovendo natriurese e diurese. No glomérulo, eles promovem dilatação da arteríola aferente e relaxamento das células mesangiais, aumentando a superfície de filtração. Nos túbulos, ANP e BNP inibem a reabsorção de sódio. Além disso, eles inibem a secreção de renina, reduzem a liberação de aldosterona, diminuem a secreção de ADH e promovem vasodilatação sistêmica.
O ANP é predominantemente armazenado e liberado rapidamente pelos átrios. O BNP, que é chamado cerebral por ter sido inicialmente isolado desse órgão, é predominantemente sintetizado nos ventrículos sob demanda, ou seja, a transcrição é induzida de forma proporcional ao estiramento.
O BNP é sintetizado como pré-pró-BNP, clivado em pró-BNP, e posteriormente dividido em BNP biologicamente ativo e NT-proBNP (fragmento inativo). O fragmento inativo é amplamente utilizado como biomarcador de doença cardíaca. Concentrações elevadas indicam estresse ventricular.
Integração estrutural e controle sistêmico
A eficiência do controle renal depende da interação entre estruturas microscópicas e sinais sistêmicos. A inervação simpática renal modula o tônus vascular e a atividade do AJG, ajustando a filtração e a retenção de fluidos em situações de demanda sistêmica. Os rins respondem aos estímulos do sistema nervoso autônomo de forma predominantemente simpática, pois a inervação parassimpática direta é mínima e funcionalmente pouco relevante. A ativação simpática promove vasoconstrição das arteríolas renais, principalmente da aferente, reduzindo o fluxo sanguíneo renal e, em estímulos intensos, a taxa de filtração glomerular. Além disso, a estimulação β₁-adrenérgica das células justaglomerulares aumenta a liberação de renina, ativando o sistema renina-angiotensina-aldosterona, o que favorece a retenção de sódio e água. O simpático também atua diretamente sobre os túbulos renais, aumentando a reabsorção tubular de Na⁺ e água e reduzindo a diurese. O sistema parassimpático não exerce efeitos diretos significativos sobre a função renal, influenciando os rins apenas de forma indireta, ao modular o tônus simpático sistêmico e a pressão arterial.Além disso, espécies como cães e gatos apresentam alta proporção de néfrons justamedulares com alças longas, uma adaptação estrutural que amplia a capacidade de concentração urinária. Por fim, a disposição anatômica da mácula densa junto ao glomérulo permite o feedback túbulo-glomerular, assegurando que cada néfron ajuste sua filtração à capacidade de reabsorção tubular.
