Filtração glomerular
Atenção: o conteúdo deste site pertence à Universidade Federal de Viçosa.
A filtração glomerular constitui a etapa inicial da formação da urina e corresponde ao movimento passivo de um ultrafiltrado do plasma a partir dos capilares glomerulares para o espaço de Bowman. O processo é considerado localmente passivo porque não há gasto direto de ATP no glomérulo para promover a filtração. Entretanto, em última análise, a força que “empurra” o fluido através da barreira de filtração, é a pressão hidrostática produzida pelo coração. Em mamíferos domésticos, o volume filtrado diariamente é muito elevado, podendo superar em dezenas de vezes o volume do fluido extracelular do animal. Essa elevada capacidade de filtração resulta da organização histológica altamente especializada do corpúsculo renal e da atuação integrada das forças físicas que regem o fluxo de fluidos através da barreira glomerular.
Barreira de filtração glomerular: Estrutura e função
A barreira de filtração glomerular (ou membrana de filtração) é formada por três camadas estruturais dispostas de maneira contínua entre o sangue e o espaço capsular. A função seletiva dessa barreira depende diretamente das características morfológicas e moleculares de cada uma dessas camadas.
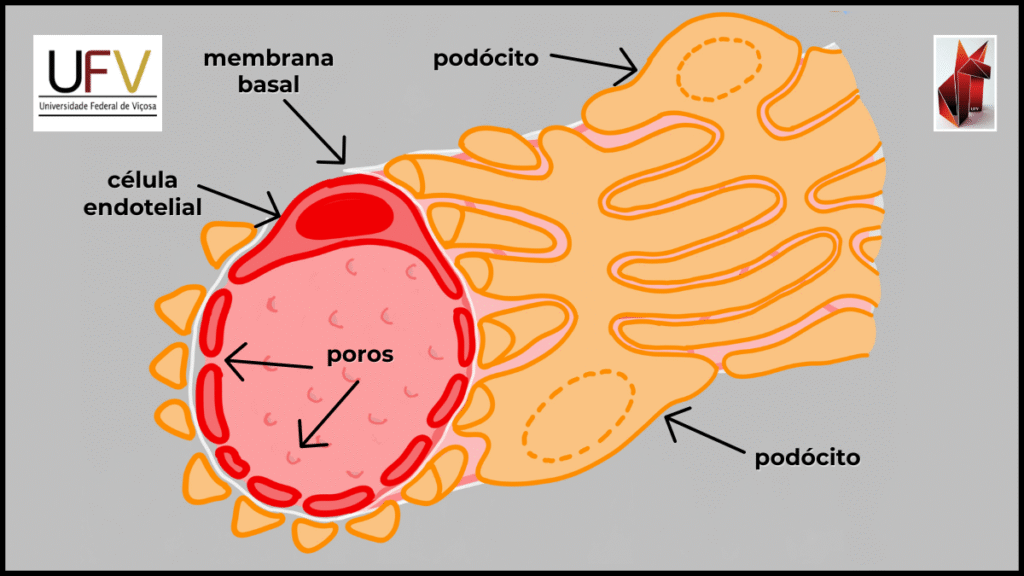
O endotélio capilar fenestrado constitui a camada mais interna. As células endoteliais são extremamente delgadas e apresentam numerosas fenestras com diâmetro entre 50 e 150 nm, o que permite a livre passagem de água e pequenos solutos. Ao mesmo tempo, a ausência de diafragmas nessas fenestras, associada à integridade celular, impede a passagem de elementos figurados do sangue, garantindo a seletividade inicial do processo.
Externamente ao endotélio encontra-se a membrana basal glomerular (MBG), uma matriz acelular espessa composta por colágeno tipo IV e glicoproteínas negativamente carregadas. A MBG organiza-se em três subcamadas (lâmina rara interna, lâmina densa e lâmina rara externa) que, em conjunto, formam uma malha física e eletrostática. Essa organização estrutural confere resistência à passagem de macromoléculas, desempenhando papel central tanto na seletividade por tamanho quanto por carga elétrica.
A camada mais externa da barreira é o epitélio visceral da cápsula de Bowman, formado por podócitos. Essas células apresentam prolongamentos citoplasmáticos primários e secundários, denominados pedicelos, que se interdigitam ao redor dos capilares glomerulares. Entre os pedicelos formam-se as fendas de filtração, recobertas por um diafragma proteico especializado. Essa arquitetura cria um sistema altamente organizado de poros finais, responsáveis pelo refinamento da seletividade do ultrafiltrado.
Aparelho justaglomerular e controle local da filtração
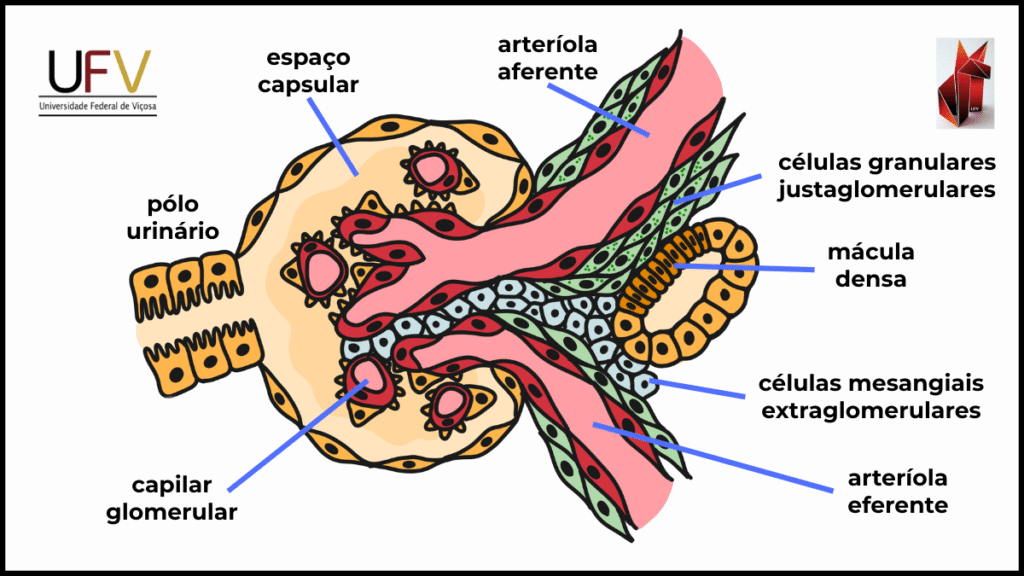
O aparelho justaglomerular (AJG) localiza-se no polo vascular do corpúsculo renal e integra elementos tubulares, vasculares e celulares especializados. Sua organização estrutural permite a regulação local da taxa de filtração glomerular em resposta a variações hemodinâmicas e à composição do fluido tubular.
A mácula densa é formada por um agrupamento de células epiteliais especializadas situadas no segmento final da alça de Henle ou no início do túbulo distal. Essas células apresentam disposição compacta e são sensíveis à concentração de NaCl no fluido tubular, funcionando como sensores da carga filtrada.
As células granulares justaglomerulares localizam-se na parede da arteríola aferente e correspondem a células de músculo liso modificadas. Sua principal característica funcional é a síntese e o armazenamento de renina, refletindo a integração entre estrutura vascular e função regulatória.
Entre a mácula densa e as arteríolas encontram-se as células mesangiais extraglomerulares, que estabelecem conexões estruturais e funcionais entre os componentes do AJG, contribuindo para a transmissão de sinais regulatórios.
Aspectos fisiológicos da filtração glomerular
A filtração glomerular não depende apenas das propriedades estruturais da barreira de filtração e das forças físicas locais, mas também da hemodinâmica renal como um todo. O rim é um órgão de elevado fluxo sanguíneo, característica fundamental para sustentar a alta taxa de filtração observada nos mamíferos domésticos. Em um animal saudável, adulto e em repouso, 20 a 25% do débito cardíaco são direcionados aos rins. Isso ocorre não porque os rins apresentam elevada demanda metabólica, mas em função de seu papel central na manutenção da homeostase do meio interno.
O fluxo sanguíneo renal (FSR) corresponde ao volume total de sangue que perfunde os rins por unidade de tempo. Como a fração do débito cardíaco dedicada aos rins é elevada, o aporte contínuo de plasma aos capilares glomerulares é garantido e a pressão hidrostática capilar se mantém elevada. Essa organização vascular singular é essencial para que o processo de filtração ocorra de forma eficiente e estável, mesmo diante de variações da pressão arterial sistêmica.
Do ponto de vista funcional, entretanto, é o fluxo plasmático renal (FPR) que se relaciona mais diretamente com a filtração glomerular. O FPR representa a fração do fluxo sanguíneo renal correspondente apenas ao plasma, excluindo os elementos figurados do sangue, que não participam do processo de filtração. O fluxo plasmático renal pode ser estimado a partir do fluxo sanguíneo renal e do hematócrito, segundo a relação FPR = FSR × (1 − Hct). O hematócrito (Hct) é a proporção do volume sanguíneo ocupada pelos elementos figurados, especialmente as hemácias. Ele pode ser determinado por um exame laboratorial e fornece informações clínicas sobre o estado hematológico do animal, sendo útil na avaliação de anemia, policitemia e alterações da volemia. Se o Hct corresponde à fração de elementos figurados, (1 – Hct) corresponde ao plasma. Assim, o FPR define a quantidade efetiva de fluido disponível para ser filtrado nos glomérulos.
A taxa de filtração glomerular (TFG) expressa o volume de filtrado formado por unidade de tempo e constitui um dos principais parâmetros da função renal. Em termos fisiológicos, a TFG resulta da interação entre o fluxo plasmático que chega ao glomérulo, as forças de Starling que regem o movimento de fluidos através da barreira de filtração e o coeficiente de ultrafiltração (Kf), que reflete a área de superfície e a permeabilidade da barreira glomerular. Alterações no calibre das arteríolas aferente e eferente modificam a pressão hidrostática capilar glomerular e, consequentemente, a TFG, evidenciando a integração entre controle vascular e função filtrante.
A relação entre o fluxo plasmático renal e a taxa de filtração glomerular é expressa pela fração de filtração (FF), definida como a proporção do plasma que é efetivamente filtrada ao atravessar os capilares glomerulares. Em condições fisiológicas, apenas uma fração do plasma que perfunde o glomérulo é filtrada, enquanto o restante segue para a circulação peritubular. Essa característica é fundamental para a dinâmica das forças de filtração, pois a remoção progressiva de água do plasma ao longo do capilar glomerular leva ao aumento gradual da concentração de proteínas plasmáticas, elevando a pressão coloidosmótica capilar (πgc) e contribuindo para a limitação da filtração ao longo do trajeto capilar.
Dessa forma, a elevada taxa de filtração glomerular observada nos rins dos mamíferos não resulta da filtração de todo o plasma que chega ao glomérulo, mas sim da combinação entre alto fluxo plasmático renal, elevada permeabilidade da barreira de filtração e manutenção de uma fração de filtração relativamente constante. Essa integração hemodinâmica assegura que grandes volumes de ultrafiltrado sejam formados diariamente, preservando ao mesmo tempo a estabilidade do meio interno e a eficiência dos processos subsequentes de reabsorção e secreção tubular.
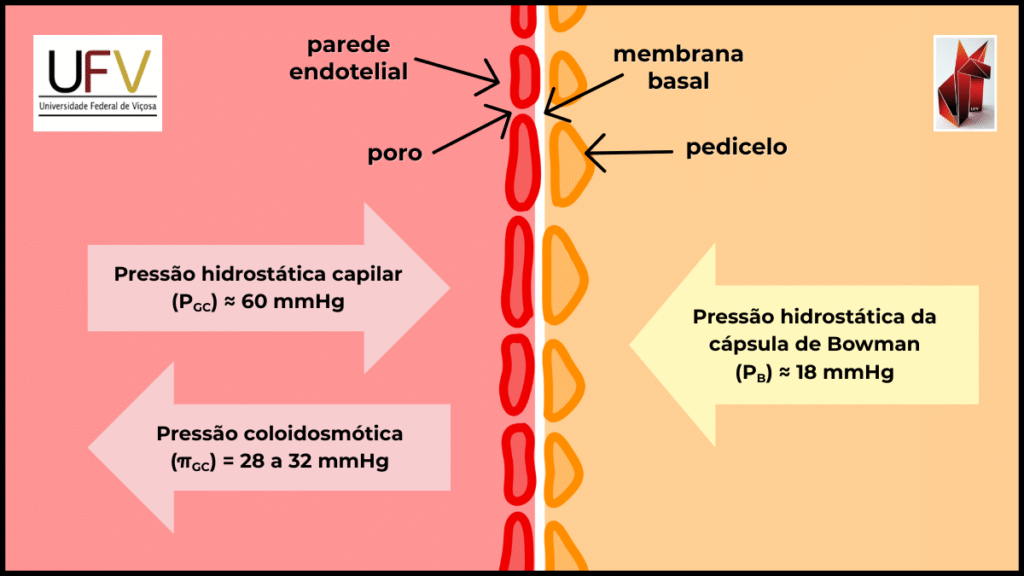
A principal força favorável à filtração é a pressão hidrostática no capilar glomerular (Pgc), mantida elevada devido à organização do leito vascular e à resistência relativa da arteríola eferente. Essa pressão impulsiona o plasma através da barreira de filtração em direção ao espaço de Bowman.
Opondo-se a esse fluxo estão a pressão hidrostática no espaço de Bowman (Pbs), exercida pelo fluido já presente no néfron, e a pressão coloidosmótica capilar (πgc), gerada pelas proteínas plasmáticas não filtradas, cuja concentração aumenta progressivamente ao longo do capilar glomerular.
Autorregulação da filtração: Integração estrutural e funcional
A estabilidade da TFG é garantida por mecanismos intrínsecos associados ao aparelho justaglomerular.
O reflexo miogênico decorre da capacidade das células musculares lisas da arteríola aferente de se contraírem quando submetidas ao estiramento provocado por aumentos da pressão arterial. Essa resposta estrutural protege os capilares glomerulares e evita variações excessivas da pressão hidrostática glomerular.
O feedback tubuloglomerular baseia-se na relação funcional entre a mácula densa e a arteríola aferente. Quando a TFG se eleva, a maior entrega de NaCl ao segmento tubular é detectada pela mácula densa, que desencadeia sinais locais levando à constrição da arteríola aferente. Como consequência, ocorre redução da pressão hidrostática glomerular e normalização da filtração.
Relações estrutura-função na eficiência da filtração glomerular
A eficiência e a seletividade da filtração glomerular dependem diretamente da integridade e das propriedades físicas da barreira. A seletividade por tamanho decorre da malha formada pela membrana basal glomerular e pelos diafragmas das fendas de filtração, que restringem a passagem de macromoléculas com raio molecular superior a aproximadamente 4 nm, ou, alternativamente, superiores a cerca de 70 kDa. Paralelamente, a seletividade por carga resulta da presença de glicoproteínas negativamente carregadas na barreira, que repelem proteínas plasmáticas aniônicas.
A extensa rede de capilares glomerulares e a alta densidade de fenestras endoteliais conferem ao glomérulo uma grande área de superfície e elevada permeabilidade, refletidas em um coeficiente de ultrafiltração (Kf) muito superior ao de outros tecidos. Por fim, a organização precisa dos podócitos, com pedicelos e diafragmas intactos, é fundamental para manter a permeabilidade controlada da barreira, assegurando que grandes volumes de plasma sejam filtrados com alta seletividade.
Composição do filtrado glomerular
O filtrado glomerular corresponde a um ultrafiltrado do plasma, cuja composição é determinada pelas propriedades físicas da barreira de filtração. A água plasmática atravessa livremente os poros da barreira glomerular, arrastando consigo os solutos que se encontram dissolvidos no plasma e cujas dimensões e carga elétrica permitem a passagem. Dessa forma, pequenos solutos hidrossolúveis, como íons (Na⁺, K⁺, Cl⁻, HCO₃⁻), glicose, aminoácidos, ureia, creatinina e outros metabólitos de baixo peso molecular, estão presentes no filtrado glomerular em concentrações aproximadamente iguais às do plasma, desde que não estejam ligados a proteínas plasmáticas.
Embora a barreira de filtração glomerular restrinja de forma altamente eficiente a passagem de proteínas plasmáticas, pequenas quantidades de proteínas de baixo peso molecular e traços de albumina podem atravessá-la em condições fisiológicas normais. No entanto, essa fração é mínima, de modo que o filtrado glomerular apresenta pressão coloidosmótica desprezível e é, do ponto de vista funcional, considerado praticamente isento de proteínas. Além disso, as proteínas filtradas são quase totalmente reabsorvidas no túbulo proximal, não contribuindo de forma significativa para a composição da urina final.
Quando a barreira não funciona: proteinúria
Se a barreira glomerular for danificada, como ocorre em uma glomerulonefrite, proteínas plasmáticas podem atravessar para o filtrado urinário. O resultado é proteinúria, perda de albumina, e pode ocorrer edema, devido à redução da pressão oncótica plasmática. Assim, entender a estrutura da barreira ajuda a compreender como pequenas alterações celulares podem gerar efeitos sistêmicos.
Quando a hemoglobina aparece na urina: hemoglobinúria
A hemoglobina é uma proteína com peso molecular inferior ao da albumina. Entretanto, em condições fisiológicas, não é encontrada no filtrado glomerular, uma vez que se encontra confinada no interior das hemácias, que são completamente impedidas de atravessar a barreira de filtração glomerular.
A presença de hemoglobina livre na urina caracteriza a hemoglobinúria e está associada a episódios de hemólise intravascular intensa. Quando ocorre lise de hemácias em pequena ou moderada magnitude, a hemoglobina liberada na circulação liga-se rapidamente à haptoglobina, uma proteína plasmática de grande tamanho molecular. O complexo hemoglobina–haptoglobina formado é volumoso e não atravessa a barreira de filtração glomerular, sendo removido da circulação principalmente pelo sistema reticuloendotelial.
Entretanto, em situações de hemólise maciça, a capacidade de ligação da haptoglobina pode ser saturada. Nessas circunstâncias, a hemoglobina livre permanece no plasma, atravessa a barreira de filtração glomerular e passa a compor o filtrado, resultando em hemoglobinúria. Assim, diferentemente da proteinúria associada a lesões da barreira glomerular, a hemoglobinúria reflete primariamente um distúrbio hematológico sistêmico, e não uma falha estrutural do glomérulo.
Quando aparecem hemácias na urina: hematúria
A hematúria caracteriza-se pela presença de hemácias intactas na urina e, diferentemente da hemoglobinúria, não resulta da filtração de componentes plasmáticos. Em condições fisiológicas, as hemácias são completamente impedidas de atravessar a barreira de filtração glomerular, tanto por seu grande tamanho quanto pela integridade estrutural do endotélio, da membrana basal glomerular e dos podócitos.
A presença de hemácias na urina indica, portanto, a existência de uma disrupção anatômica ao longo do trato urinário, que pode ocorrer no glomérulo, nos túbulos, na pelve renal, nos ureteres, na bexiga ou na uretra. Quando a origem é glomerular, a hematúria está geralmente associada a lesões estruturais da barreira de filtração, permitindo a passagem de células sanguíneas para o espaço de Bowman.Do ponto de vista fisiopatológico, a hematúria difere tanto da proteinúria quanto da hemoglobinúria. Enquanto a proteinúria reflete aumento da permeabilidade da barreira glomerular a macromoléculas plasmáticas e a hemoglobinúria resulta de hemólise intravascular intensa, a hematúria representa a perda direta de células sanguíneas inteiras, indicando ruptura ou inflamação tecidual no sistema urinário.
